۱الف) در باره سختی جامدهای یونی می توان سه قاعده زیر موسوم به قاعده Fajans را بیان کرد:
1) در جامدهای یونی با ساختار بلوری یکسان و بار برابر، هر چه فاصله بین یونها کمتر باشد، بر میزان سختی بلور افزوده میشود.
2) در جامدهای یونی که ساختار یکسان و فاصله بینیونی نزدیک دارند، با افزایش بار آنیون و کاتیون، سختی بلور افزایش مییابد.
3) چنانچه یونها در یک جامد یونی دارای آرایش گاز بیاثر
باشند، نسبت به جامدهای یونی دیگر که در آنها یونها آرایش گاز بیاثر
ندارند، (در صورتی که بار، فاصله بینیونی و ساختار بلور یکسان باشند.)
سختی بلور بیشتر است.
۲الف) سیتریک اسید، سدیم کربنات، جوش شیرین (سدیم بیکربنات)،
سولفوریک اسید، دی اکسید کربن، هیدروژن پراکسید، آمونیوم پرکلرات، پتاسیم
یدید، الکلها و... به عنوان سوخت شیمیایی خودروهای کوچک استفاده میشوند.
چند واکنش از این دست عبارتند از:
2HOOH --> 2 H2O + O2 enzyme: catalyses
H2CO3 --> CO2 + H2O enzyme: carbonic anhydride
در واکنشهای بالا که با استفاده از آنزیم انجامپذیرند، از انرژی به دست آمده از شکستن پیوند استفاده میشود.
سوختن اتانول:
C2H5OH + 3 O2 --> 2 CO2 + 3 H2O
تجزیه اسید استیک:
CH3CO2H --> CO2 + CH4
یا تجزیه جوش شیرین:
2NaHCO3 --> Na2CO3 + CO2 + H2O
دو واکنش اخیر برای شروع به گرما نیاز دارند اما پس از شروع واکنش، گرماده هستند.
۳الف) کلرید آهنIII یا FeCl3، مادهای به شدت سمی، خورنده و
اسیدی با رنگ متغیر است که رنگ آن به زاویه دید بستگی دارد و از سبز تیره
تا بنفش تغییر میکند. انحلال آن در آب گرمازاست و در اثر انحلال، محلول
قهوهای رنگ و اسیدی میدهد. در اثر گرما، به کلرید آهنII و گاز سمی کلر
تجزیه میشود:
FeCl3 + Q --> FeCl2 + 1/2 Cl2
با ترکیب FeCl3، جوش شیرین و آب در یک بطری میتوان گازی
فوقالعادهای تولید کرد که سبب میشود بطری نوشابه را مانند موشک پرتاب
کند.
یادآوری میشود هر ماده منفجره به دو جزء ماده سوختنی و
اکسنده نیاز دارد. برای مثال پتاسیم نیترات به شدت اکسنده است ولی به
تنهایی منفجر نمیشود. اما ترکیب چهار به شش شکر (به عنوان ماده سوختنی) و
پتاسیم نیترات به یک بمب دودزا منتهی میشود.
۴الف) فسفید فلزهایی مانند آلومینیوم، روی، کلسیم و منیزیم به
عنوان یک گونه از سمهای دفع آفات، حشرات و جوندهها از دیرباز در بسیاری
از کشورهای دنیا به کار میرفتهاند که قیمت ارزان، کاربرد آسان و کارآیی
بالا موجب مصرف گسترده آنها در کشاورزی شده است.
در ایران "فسفید آلومینیم" با نام قرص برنج به ویژه در شمال
کشور برای نگهداری برنج در انبارها و جلوگیری از تخریب آن توسط حشرهها از
سالیان گذشته استفاده میشده است.
قرصهای برنج در تماس با رطوبت موجود در برنج و غلات دیگر، گاز
سمی فسفین آزاد میکنند که این گاز موجب نابودی آفات و حشرهها و
ماندگاری محصول در انبار میشود. به علت فراریت و نیمه عمر کوتاه گاز فسفین
در محیط، مصرف برنج و دیگر فراوردههای کشاورزی نگهداریشده توسط این
ماده، پیامدهای سوء در انسان ندارد.
البته فسفید آلومینیوم جزو سمهای کشنده برای انسان است و
مقدار کشنده آن برای انسان بالغ با میانگین وزن 70 کگ حدود 500 میلیگرم
برآورد شده، این در حالی است که هر قرص برنج حاوی یک گرم فسفید آلومینیوم
است. فسفید آلومینیوم در معده در اثر واکنش با آب و اسید معده گاز سمی
فسفین آزاد میکند و نشانههای مسمومیت شامل طیف وسیعی از آشفتگیهای
گوارشی، قلبی عروقی، کلیوی، کبدی، عصبی و تنفسی است که میتوان استفراغ ،
درد ناحیه شکم، سرگیجه، کاهش هوشیاری، کاهش فشار خون، بینظمی تپش قلب،
زردی، تشنج و بیهوشی را نام برد.
توضیح بیشتر درباره سمپاشی: دوره کارنس به زبان ساده عبارت
است از مدت زمانی که پس از سمپاشی باید طی شود تا فراورده کشاورزی را
بتوان مصرف کرد. مسلما پس از سمپاشی نه تنها بافتهای بیرونی گیاه و
میوهها به سم آغشته میگردند بلکه پارهای از سمها از طریق روزنههای گیاه
یا آوندهای چوبی و آبکش به بافتهای درونی نفوذ و به همه نقاط گیاه سرایت
میکنند که مصرف چنین فراوردهای برای بدن زیانآور است.
۵الف) پتاسیم نیترات KNO3 یک ترکیب یونی به رنگ سفید و در آب
محلول است. پتاسیم نیترات کاربردهای فراوان دارد که از جمله برای ساختن
باروت و نیز در ترکیب خمیر دندان به کار میرود. واكنش انفجار باروت سیاه
را میتوان به این صورت نوشت:
4KNO3 + S + 4 C -> 2 N2 (g) + 2 K2O + 4 CO2 (g) + SO2 (g)
برخی واكنش انفجار باروت را در فضای محدود به صورت زیر نوشتهاند:
2KNO3 + S + 3 C -> N2 + 3 CO2 + K2S
هنگام انفجار دودی خارج میشود كه مربوط به ایجاد پتاسیم سولفید است.
اگر در هوای آزاد باروت را بسوزانیم معادله واكنش چنین است:
4KNO3 + 3 S + 2 C -> 2 N2 + 2 K2CO3 + 3 SO2
در عمل برای ساخت باروت سیاه 75 درصد پتاسیم نیترات، 14 درصد
زغال چوب و 11 درصد گوگرد به كار میرود. پتاسیم نیترات (شوره) همان ماده
سفید رنگی است كه به طور طبیعی در كنار دیوارهای مرطوب ایجاد میشود.
پتاسیم نیترات همچنین به عنوان یک ماده اکسنده نیز کاربرد دارد.
٦الف) چرا با این که ظرفیت کربن 4 و کلسیم 2 است، فرمول کلسیم کاربید به صورت CaC2 نوشته میشود؟
پاسخ: ظرفیت 4 اتم کربن در پیوندهای اتمی دیده میشود، درحالی که در این جا یک پیوند یونی وجود دارد.
در دمای معمولی، کلسیم و کربن با هم واکنش نمیدهند. در اثر
افزایش دما تا حدود 2000 درجه سانتیگراد و در اثر واکنش آهک و کک، کلسیم
کاربید به دست میآید. در این ترکیب یونی، C+4 وجود ندارد بلکه آنیون C2 با
دو بار منفی وجود دارد، یعنی دو اتم کربن که با پیوند سه گانه به هم پیوند
شدهاند و بار کلی آن 2- میباشد. سپس این آنیون دو اتمی با دو بار منفی
میتواند با یک کاتیون کلسیم واکنش بدهد و ترکیب CaC2 به دست آید:
CaO + 3 C --> CaC2 + CO
به طور کلی از واكنش مستقیم كربن با فلزها یا اكسید فلزها در
دمای بالا تركیباتی به دست میآیند كه كاربید نامیده میشوند. كاربیدها
دارای یون C=2 هستند.
7الف) اجزای اصلی تشکیلدهنده شیشه
با نگاه به جدول
عناصر، کمتر عنصری را میتوان یافت که از آن شیشه به دست نیاید. ولی سه
ماده کربنات دو سود، سنگ آهک و سیلیس مواد اصلی تشکیلدهنده شیشه میباشند.
مواد شیشهساز مورد تایید موسسه استاندارد عبارتند از سیلیس، دی اکسید
بور، پنتا اکسید فسفر که از هـر یک به تنهایی میتوان شیشه تهیه کرد.
گداز آورها:
کربنات
سدیم، کربنات پتاسیم و خردهشـیشـه، سـیلـیکات سدیم و سـلـیـس گدازآور
میباشند، در آب حل میشوند و از شفافیت شیشه به تدریج کم میکنند به هـمین
عـلـت است که بیشتر شیشههای مصرفشده در گـلخانه پس از چند سال کدر
میشوند و نور از آنها به خوبی عـبور نمیکند.
تثبیتکنندهها:
برای
آن که مقاومت شـیشـه را در برابر آب و هـوا ثابت کنند باید اکسـیدهای
باریم، سرب، کـلسیم، مـنـیزیم و روی به مـخـلـوط شیشه افزوده شود که به
آنها ثابتکـننده میگـویند.
تصفـیهکنندهها:
تصفیهکنندهها موجب کاستن حباب هوا در شیشه میشوند و بر دو نوعند:
الف) فـیزیکی: سولفات سدیم، کلرات سدیم با ایجاد حبابهای بزرگ، حبابهای کوچک را جذب و از شیشه مذاب خارج میکنند.
ب) شیمیایی: املاح آرسنیک و آنتیموان ترکیباتی ایجاد میکنند که حبابهای کوچک درون شیشه را از بین میبرند.
تا
این جا به موادی اشاره شد که نبودشان در مواد اولیه از مرغـوبیت کالا
میکاهد. حال به چند ماده دیگر که به نوعـی در تولید شیشه سهیم هستند،
اشاره میشود.
افزودنیها
1) استفاده از بوراکس به جای اکسید و
کربنات سدیم ( گدارآور ) که در اثر گرما به سدیم اکسید و بورم اکسید تجزیه
میشود و در واقع به جای هر دو ماده عمل میکند.
2) استفاده از نیترات سدیم برای از بین بردن رنگ سبز شیشه (ناشی از اکسید آهن که همراه مواد دیگر وارد کوره میشود.)
3) استفاده از اکسید منگنز که باعـث مقاومت بیشتر در برابر عـوامل جوی و شفافتر شدن شیشه میشود.
4) استفاده از اکسید سرب به جای کلسیم اکسید برای ساختن شیشههای مرغـوب بلور که سبب درخشندگی شیشه میشوند.
5) اکسـید نقـره برای ساختن بلور مرغـوب.
6) فلدسپار که مقاومت شیشه را در برابر مواد شیمیایی افزایش میدهد.
7) برای این که شیشه در برابر اسید فلوئوریدریک هم مقاوم باشد، ترکیباتی از فـسـفـات به آن می افزایند.
8) خردهشیشه که به ذوب مواد سرعت بیشتری می دهد.
9) اکسید فلزات برای تهیه شیشههای رنگی.
10) اکسید سزیم برای جذب پرتو فروسرخ استفاده میشود.
انواع شیشه و کاربرد آنها
شیشه رنگی
به دو طریق میتوان شیشه رنگی به دست آورد"
1.
با افـزودن و کم کردن برخی مواد شیمیایی در مصالح اولیه تهیه شیشه. برای
نمونه اکسیدهای مسی به شیشه رنگ قرمز میدهند و رنگ آبی پر رنگ به وسیله
اکسید کبالت به دست میآید. رنگ زرد نیز با افزودن اکسید اورانیوم و
کادمیوم حاصل میشود.
2. شیشه سفید را در شیشه مذاب رنگی فـرو میکنند
تا دو روی آن رنگی شود. شیشههای رنگی در ویترین مغازهها، نمایشگاهها،
آزمایشگاهها و ساختمانهای صنعتی به کار میروند.
شیشه ضد آتش (پیرکس)
همراه مواد اولیه این شیشهها که مقاومت زیادی
در برابر گرما دارند، مقدار زیادی اکـسـید بوریک (بوراکس) به کار میرود و
سـیلـیس آنها از انواع شیـشـههای معمولی بیشتر است. از آنها معمولا به
عنوان ظرفهای آزمایشگاهی و آشپزخانه و یا در جلوی بخاریهای دیواری و
اجاقها استفاده مینمایند.
ویژگی نشکن در شیشههای پیرکس با نوعی
عملیات گرمایی تنشزدایی ایجاد میشود. برای این کار، شیشه تا دمای 620 تا
630 درجه گرم میشود و به حالت خمیرگونه در میآید و در فشار خاصی ناگهان
سرد میشود.
شیشه مسطح
این نوع شیشه را با اضافه نمودن توری فلزی میان شیشه
میسازند و بیشـتر برای درهای ورودی، کارگاهها، موتورخانهها، آسانبرها و
هـر جایی که خطر شکـسـتن و فرو ریختن شیشه وجود دارد، استفاده مینمایند.
شیشه دو جداره
شیشه دو جداره از دو لایه ساده و گاهی رنگی که به
موازات یکدیگر قرار گرفتهاند، ساخته شده است. فضای بین آنها با مواد
خشککنندهای مانند سیلـیکاژل پر یا بین دو لایه خلا ایجاد میشود. این نوع
شیشه که عایق گرما، سرما و صداست در بسیاری از ساختمانها مانند
فرودگاهها، هتلها و بیمارستانها به کار میرود.
شیشه سکوریت (securit)
برای تولید شیشه سکوریت، شیشه تا دمای حدود
700 درجه سانتیگراد گرم و به طور ناگهانی و در شرایط خاص سـرد میشود. این
کار مقاومت شیشه را در برابر ضربه و نیز شوکهای گرمایی حدود 3 تا 5 برابر
افزایش میدهد. این شیشهها در صورت شکستن، به ذرات ریز و مکعبی تقسیم
میشوند که آسیب نمیرسانند. از این نوع شـیشـه در ویترین فروشگاهها،
درهای شـیشـهای و پنجرههای جانبی خودروها استفاده میشود.
شیشه نشکن
این نوع شیشهها شامل دو یا چند لایه شیشهاند که به
وسیله ورقههایی از نایلون شفاف تحت فشار و گرما به هم میچسبند. همچنین
برخی از انواع شیشههای طلقدار به عنوان عایق صوتی، جاذب گرما، کاهنده
شفافیت و شیشه ایمنی به کار برده میشوند. وقتی این شیشهها میشکنند،
خاصیت کشسانی نایلون، از پخش و پراکندگی ذرات شیشه جلوگیری میکند. این نوع
شیشهها در خودروها و ویترین مغازههایی که اشیای گرانقیمت میفروشند به
کار میروند. ممکن است شیشه نشکن از جنس شیشه سکوریت ساخته شود.
شیشه بازتابنده (reflex)
در این نوع شیشهها، یک سطح شیشه با یک پوشش
بازتابنده نور و گرما و از جنس فلز یا اکسید فلزی پوشانده میشود. این نوع
شیشهها، نور خورشید را باز میتابانند و سبب کاهش دما و درخشندگی نور
میشوند. اگر در روشنایی روز از بیرون به شیشه بازتابنده نگاه کنیم تصاویر
بیرون را مانند آینه باز میتاباند و اگر از درون نگاه کنیم شیشه شفاف
خواهد بود. این پدیده شبها برعکس است؛ یعنی شیشه از بیرون شفاف و از درون
مانند آینه است. این شیشه با بازتابش نور خورشید، گرمای ناشی از تابش
خورشید را کاهش میدهد و در نتیجه سبب صرفهجویی در هزینههای ساخت،
راهاندازی و نگهداری دستگاههای تهویه و تبدیل میشود.
٨الف) براي تميز کردن آلومينيومي که رنگ آن کدر شده است، چون روي آن يک
لايه از اکسيد آلومينيوم وجود دارد، ميتوان آن را در محلول سود و سپس برای
از بین بردن دوده، در محلول اسيد نيتريک غوطهور کرد.
در اثر اکنش سود با اکسيد آلومينيوم (Al2O3) خواهیم داشت:
Al2O3 + 6 NaOH --> 2 Al(OH)3 + 3 Na2O
اما Al(OH)3 وارد اين واکنش ميشود:
Al(OH)3 + NaOH --> NaAlO2 + 2 H2O
بنا بر اين، واکنش نهايي به صورت زير نوشته ميشود:
Al2O3 + 2 NaOH --> 2 Na[Al(O2)] + H2O
واکنش بين نيتريک اسيد و کربن (دوده) نيز به صورت زير است:
C + 4 HNO3 = CO2 + 4 NO2 + 2 H2O
توضیح بیشتر: آلومینیم اكسید یك تركیب آمفوتر است، یعنی در برابر
اسیدها، نقش باز و در برابر بازها، نقش اسید را ایفا میكند. واكنش این
ماده در محیطهای اسیدی قوی یا قلیایی قوی به صورت زیر میباشد:
Al2O3 + 6 HCl --> 2 AlCl3 + H2O
همچنین در محیط قلیایی قوی:
Al2O3 + 2 NaOH + 3 H2O --> Na[Al(OH)4]
در pHهای میانی تركیبهای دیگری نیز به دست میآیند. برای مثال وقتی pH
بالا در سدیم هیدروكسید کاهش یابد، به جای تركیب Al(OH)4 با یك بار منفی،
تركیبهای Al(OH)3 و Al(OH)+2 به دست میآیند؛ با ادامه كاهش pH، Al(OH)+2
تولید میشود تا این كه در اسیدی قوی تركیب Al+3 را داریم كه در حضور هیدرو
كلریك اسید به صورت AlCl3 در میآید.
٩الف) پنبه نسوز (آزبست) از استخراج تخته سنگهاي ليفي به دست ميآيد.
طول الياف آزبست از 25 ميليمتر بیشتر نمیشود. رنگ آن بين سفيد و خاكستري
متغير ميباشد. پنبه نسوز عايق گرما و جريان برق است و مواد شيميايي نيز بر
روي آن اثری ندارند. بدين جهت براي عايقبندي و همچنين تهيه لباس
آتشنشانان به کار میرود. در معبدهاي قديمي فتيله مشعلها را از پنبه نسوز
ميساختند و روميان خاكستر مردههايي را كه میسوزاندند، در لفافي از پنبه
نسوز ميپيچيدند و از آن نگهداري ميكردند.
پنبه نسوز بیشتر از موادي
مانند سيليكاتهاي آهك و اكسيد منيزيم تشكيل شده است و در آن آهن هم يافت
ميشود. پنبه نسوز شبيه پشم و پنبه معمولي است، با اين تفاوت كه در برابر
آتش مقاومت ميكند. در حالي كه پشم و پنبه اين خاصيت را ندارند. همچنين
پنبه نسوز را میريسند و به صورت نخ در ميآورند و با آن پارچه میسازند.
كارگراني كه در كارخانهها با خطر آتشسوزي روبرو هستند كلاهخود، دستكش،
لباس و چكمههايي از جنس پنبه نسوز دارند. پنبه نسوز تا دمای 1100 تا 1600
درجه سانتيگراد را تحمل ميكند و برخي از انواع آنها حتا تا 2800 درجه
نيز مقاومت ميكنند.
پنبه نسوز در رگههاي برخي صخرهها يافت ميشود و
براي استخراج يك تن از آن بايد در 50 صخره حفاري و كاوش كنند. در كشور
كانادا حدود 75 درصد از پنبه نسوز خام جهان توليد ميشود.
البته به یاد داشته باشید، آزبست سرطانزاست.
١٠الف) در انرژی شبکه، بار یون نقش مهمتری از اندازه یون دارد زیرا با
افزایش بار یون، جاذبه الکتروستاتیک بین یونها افزایش مییابد. همچنین بار
کاتیون و بار آنیون به یک اندازه نقش دارند، زیرا میزان بار یون یا همان
قدر مطلق بار مهم است و منفی یا مثبت بودن آن تفاوتی ندارد.
از این رو،
برای تعیین انرژی شبکه هر چه بار یونها بیشتر باشد (چگالی بار بیشتری داشته
باشند.) انرژی شبکه بیشتر میشود. اگر بار یونها برابر باشد، هرچه شعاع
یونها کوچکتر باشد چگالی بار آنها بیشتر است و بنا بر این انرژی شبکه بیشتر
میشود.
١١الف) به طور كلی زاجها، نمكهای دوگانه سولفات هستند. (نمك دوگانه نمكی
است كه در آن یك بنیان آنیونی با دو نوع كاتیون در بلور شركت میكند.)
فرمول عمومی آنها
M[Al(SO4)2].12H2O
میباشد كه در آن M یک كاتیون تك اتمی و تک بار غیر از +Li
است. (چون یون +Li كوچك است و سبب ناپایداری کملکس میشود.) برای مثال زاج
پتاسیم، KAl(SO4)2.12H2O با جرم مولكولی 474 گرم بر مول میباشد.
زاجها را برای انداختن ترشی و شور، تصفیه آب و پساب، سیمان ضد آب، كاغذ سازی و به عنوان كفساز در كفهای آتشنشانی به كار میبرند.
زاجهای
رنگی، نامهاییاند كه به برخی از نمكهای سولفات فلزها (به علت رنگ آنها)
نسبت میدهند. برای مثال، مس II سولفات (CuSO4,5H2O) را زاج آبی، منیزیم
سولفات (MgSO4.7H2O) را زاج سرخ یا نمك اپسوم و نیز آهن II سولفات
(FeSO4.7H2O) را زاج سبز مینامند.
روش تهیه اسید سولفوریک از زاج سبز:
نخست
زاج سبز FeSO4.7H2O را گرما میدهند تا همه آب تبلور آن تبخیر شود و FeSO4
به دست آید. با گرمادهی بیشتر، FeSO4 به Fe2O3 و اکسیدهای گوگرد تجزیه
میشود که با ادامه گرمادهی، تری اکسید گوگرد به اکسیژن و دی اکسید گوگرد
تبدیل میشود.
FeSO4.7H2O --> FeSO4.H2O --> FeSO4
2FeSO4 --> Fe2O3 + SO2 + SO3
SO3 --> 2SO2 + O2
البته اگر زاج سبز را گرم کنیم تا سولفات آهن II بیآب به دست آید، چون
این ماده به آسانی در آب حل میشود، میتوان آن را در آب حل نمود و اسید
سولفوریک به دست آورد:
FeSO4 + H2O --> H2SO4 + FeO
كات كبود (سولفات مس II) یا زاج آبی دارای فرمول CuSO4,5H2O میباشد كه
از واكنش سولفوریك اسید با اكسید مس طی عمل تبلور تهیه میشود و كاربرد آن
در كشاورزی برای آفاتزدایی، تصفیه آب و ماده نگهدارنده چوب میباشد. كات
كبود نیز به دلیل خواص مولكولی خود از رشد جلبكها جلوگیری میکند و به همین
دلیل هنگام ذخیره آب تصفیهشده به آب میافزایند. كات كبود همچنین در
دباغی پوست و نیز در رنگسازی و ساخت ابریشم به کار میرود. حلالیت این
ماده در آب برابر 6/31 گرم در 100 سی سی آب در دمای صفر درجه سانتیگراد
میباشد.
توضیح بیشتر: آب در زاج و بسیاری از نمکهای متبلور وجود دارد.
آب میتواند تنها در بیرون از مولکول، آن را آبپوشی نماید و یا میتواند
درون ترکیب وارد شود و با آن پیوند بدهد که در این حالت آب تبلور نامیده
میشود؛ به عبارت دیگر، آب تبلور آبی است كه به همراه بلور برخی جامدهای
یونی است.
هنگامی كه یك جامد یونی از محلول آبی متبلور میشود، ممکن
است شماری از مولكولهای آب در شبكه بلور به دام بیفتند و با بلور پیوندهای
ضعیف واندروالس بدهند. برای مثال، باریم كلرید در آب محلول است و میتوان
به وسیله تبخیر محلول و اشباع كردن آن، مقداری بلور BaCl2 به دست آورد. در
این حالت، به جای BaCl2 خالص، نمك متبلور آن را داریم که فرمول آن
BaCl2,2H2O میباشد. به این گونه بلورهای نمكی كه با مولكولهای آب همراه
هستند، هیدراته و به آبی كه در شبكه بلوری این نمكها وارد شده است، آب
تبلور گفته میشود. مثال دیگر از این دست، سولفات مس آبدار است كه دارای 5
مولكول آب تبلور میباشد: CuSO4,5H2O
هیدراتها بر اثر گرم شدن آب تبلور خود را به صورت بخار آب از دست میدهند.
BaCl2,2H2O (s) + Q --> BaCl2 (s) + 2 H2O (g)
از بین رفتن آب تبلور یك نمک آبدار را شكوفا شدن مینامند.
به طور
معمول، هیدراتها بلورهای بزرگ و شفاف تشكیل میدهند. رنگ برخی از نمكهای
آبدار با رنگ نمك بیآب آنها متفاوت است، از این رو، از این نمكها به
عنوان شناساگر رطوبت استفاده میكنند. برای مثال:
قرمز رنگ CoCl2.2H2O
صورتی رنگ CoCl2.5H2O
بنفش رنگ CoCl2.4H2O
آبی رنگ CoCl2
١٢الف) کف چه اشکالي دارد؟
کف پراکندگي پايدار تودهاي از حبابهاي
تشکيلشده از گازها (بیشتر هوا) در يک مايع ميباشد. به ندرت مشاهده گرديده
که يک محصول خالص داراي کف باشد. غیر از مخلوط هيدروکربنها که علت توليد
کف ايزومرها ميباشند، اساساً تشکيل کف به عامل فعال سطحي (surfactant)
بستگی دارد.
کف ناپايدار است و در يک محلول بدون اعمال هيچ گونه نيروي
بيروني کفهاي توليدي متلاشي و به مايع تبديل خواهند شد. جذب يک عامل
افزاينده کشش سطحي، از اين تخريب جلوگیری ميکند. ميتوان گفت تقريباً در
هر مايعي با توجه به انتخاب درست يک فعال سطحي يا گاز تزريقي کف متفاوتي
خواهيم داشت. در مايعات ويسکوزتر، کف پايداري بيشتري دارد.
تئوري ضد کف
عملکرد
ضد کفها به دو صورت است: به صورت کاهش کشش سطحي و تخريب عوامل
تثبيتکننده سطوح بیرونی حبابها و يا ترکاندن حبابها به صورت موضعي.
تخريب عوامل تثبيتکننده، به نوع کف و ميزان کشش سطحي مايع بستگی دارد. کم
بودن کشش سطحي ضدکف نسبت به کف توليدي داراي اهميت ميباشد.
اثر
پراکندگي ضدکف هنگامی خود را بروز ميدهد که به مواد فعال سطحي اين اجازه
را بدهد که بيشتر به سمت قسمتهاي داراي کف هدايت شوند. در نمونههاي داراي
امولسيون، پودرهاي پرکنندهاي مانند سيليکا و منگنز به کار میروند؛ اين
پرکنندهها به عنوان يک عامل فعالکننده سطحي، به پراکندگي حبابها و
ترکاندن حبابهاي کف کمک ميکنند.
انواع ضد کف
ضد کفها دو نوعند: 1) پايه سيليکوني 2) پايه معدني
ضد
کف پايه معدني بیشتر در رنگ، جوهر و صنايع پوششدهنده به کار میرود. به
علت کاهش کشش سطحي سيليکون در سطوح معيوب، از اين نوع ضدکف نبايد استفاده
کرد.
ضد کفهای سيليکوني براي نمونههاي روغني:
بهترين نمونه،
ترکيبات سيليکوني CAF1000C است که شامل ادتيوهايي با بازده خيلي بالا در
سيالات ميباشد. هنگام استفاده از يک سيال، سرعت و مدت زمان ترکيدن
حبابها، عامل مهم برای انتخاب ضدکف ميباشد. کف سيالات با ويسکوزيته
پايين، سريعتر ميترکد و ضدکف سيالات با ويسکوزيته بالاتر در زمان
طولانيتر خاصيت خود را نشان ميدهد که در اين مورد CF12.5K مناسب ميباشد.
ضدکفهای سيليکوني براي نمونههاي آبي:
ضدکفهاي سيليکوني معمولاً در دو نوعِ خوراکي و صنعتي دستهبندي ميگردند و در امولسيونهاي 10، 20 و 30 درصدي موجود ميباشند.
ضدکفهاي صنعتي
ضدکفهاي صنعتي به دو صورت عمل ميکنند:
1- در هنگام افزودن به نمونه، حبابها را به سرعت ترکانده و حذف ميکنند.
2- در درازمدت، حضورشان مانع تشکيل دوباره کف ميگردند.
نمونههاي
CAF100,200,300 هر دو خاصيت یادشده را دارند. نمونههاي ديگر مانند CAF505
که قيمت کمتري دارند، برای پسابهاي صنعتي به کار میروند. اگر ضدکف غير
سيليکوني مورد نياز باشد نمونههاي CNS672,775,890 سفارش ميگردد. براي
نمونههاي خشک مانند پودرهاي شوينده، نوع CAF1100 را ميتوان قبل از مخلوط
کردن اضافه نمود.
ضدکفهاي خوراکي
ضدکفهاي سيليکوني پايه خوراکي Flexichem توسط مصوبه افزودنيهاي مجاز خوراکي فرموله گرديدهاند.
وسايل
به کار گرفتهشده جهت استفاده از ضدکف قبل از کاربرد استريل ميگردند. همه
وسايلِ در تماس با ضدکف بايستي جهت اطمينان و تأييد استانداردهاي سلامتي و
عدم وجود ذرات ريزي مانند باکتريها تست گردند.
همه ضدکفهاي خوراکي CFA110,210,310,100C بدين روش تهيه شدهاند.
١٣الف) روش شناسایی طلای تقلبی: طلا تنها با تيزاب سلطاني واكنش ميدهد
يعني مخلوطي از نيتريک اسيد و هيدروکلريک اسيد با نسبت سه به یک. به همين
خاطر چنانچه فلزي با نيتريک اسيد يا سولفوريک اسيد گرم و غليظ واکنش داد،
طلا نیست و چنانچه با يکي از اين دو اسيد واکنش نداد، طلا ميباشد.
اما طلافروشان از روشهاي ساده و به کمک تجربه يا خراشاندن طلا و ديدن رنگ آن استفاده ميکنند.
١٤الف) اگر اختلاف الکترونگاتیوی بین دو عنصر
کمتر از 4/0 باشد، پیوند کوالانسی غیرقطبی است: H2
کمتر از 7/1 باشد، پیوند کوالانسی قطبی است: NaCl
کمتر از 9/1 باشد، پیوند یونی است: HCl
15الف) تیتراسیون اکسایش کاهش
در تیتراسیونهای معمولی مانند
تیتراسیونهای خثی شدن، یک اسید با غلظت نامعین، به وسیله بازی با غلظت
معین تیتر میشود. نقطه همارزی، نقطهای است که در آن تعداد یونهای +H با
تعداد یونهای – OH همارز یا برابر میشود. یک شناساگر به محلول اضافه
میشود که در pH خنثی تغییر رنگ میدهد. در این زمان، افزودن باز قطع
میشود و از روی مقدار حجم مصرفی باز، غلظت اسید با حجم معین را میتوان
محاسبه نمود.
تیتراسیونهای اکسایش کاهش بر پایه انتقال الکترون بنا
شدهاند. در تیتراسیونهای اکسایشکاهش، یک جسم کاهنده را میتوان توسط
محلول استاندارد یک جسم اکسنده تیتر نمود. عکس این عمل نیز صادق است، یعنی
یک جسم اکسنده را میتوان توسط محلول استاندارد یک جسم کاهنده تیتر نمود.
بنابراین فرمول کلی این تیتراسیونها عبارت است از:
aOX2 + bRed1 ---> aRed2 + bOX1
a و b ضرایب اجسام اکسنده و کاهنده است. در یک واکنش اکسایشکاهش، هر چه
تفاوت پتانسیل استاندارد E zero برای نیمواکنشهای اکسایش و کاهش بیشتر
باشد، واکنش کاملتر است و این واکنشها در تیتراسیونها اهمیت بیشتری
دارند.
اکسندههای مهم که از محلول استاندارد آنها بیشتر استفاده
میشود، عبارتند از: ید، پتاسیم پرمنگنات، سریک سولفات، پتاسیم بیکرومات و
پتاسیم یدات.کاهندههای مهم عبارتند از: سدیم تیو سولفات که از محلول
استاندارد آن در یدومتری استفاده میشود، و نیز محلول استاندارد انیدرید
آرسینو 2O3As.
بعضی از واکنشهای اکسایشکاهش را بر حسب نام استاندارد به کار برده شده نامگذاری کردهاند مانند:
1- منگانومتری به تیتراسیونهای اکسایشکاهش که از پرمنگنات پتاسیم به عنوان اکسنده استفاده میشود، گفته میشود.
2-
ید سنجی یا یدومتری: به طور کلی به واکنشهایی که در آن ید اکسید میگردد،
یعنی ید از محلول یدیدها آزاد میگردد یدومتری گویند. روشهای زیادی بر
اساس خواص کاهندگی یون یدید استوارند. ید که محصول واکنش است، معمولاً با
محلول استاندارد تیوسولفات در حضور شناساگر چسب نشاسته تیتر میشود.
3- کروماتومتری: در این روش یک جسم کاهنده توسط محلول استاندارد پتاسیم بیکرومات اکسید شده و تعیین مقدار میگردد.
4- بروماتومتری: مستلزم اکسیداسیون با پتاسیم برومات توسط یونهای 4Ce+ میباشد.
بیشتر
شناساگرهای مورد استفاده در تیتراسیونهای اکسایشکاهش خود عوامل اکسنده
یا کاهندهاند که به جای حساس بودن به تغییر غلظت، نسبت به تغییر پتانسیل
سیستم پاسخ میدهند.
16الف) آب، شرط وجود زندگی میباشد و بیشتر واکنشهای شیمیایی در
محیط آبی روی میدهند. آب به علت برخی ویژگیها از تغییرات ناگهانی دمای
طبیعت جلوگیری میکند. آب، پس از مصارف گوناگون (خانگی، کشاورزی، صنعتی و…)
به پساب تبدیل میشود. برای جلوگیری از آلودگی آب و محیط زیست توسط این
پسابها باید راهکارهایی برای تصفیه و استفاده دوباره از آنها به کار برد.
پسابهای صنعتی
پسابهای
صنعتی از صنایع گوناگون پدید میآیند و بسته به نوع صنایع، ترکیب شیمیایی
دیگر گون دارند و وقتی وارد دریاها میشوند، آب را آلوده میکنند و آبزیان
را میمیرانند.
مواد شیمیایی موجود در پسابهای صنعتی
بسته به نوع
کارخانهها و فراوردههای آنها، ترکیبهای شیمیایی و درصد آنها در
پسابهای صنعتی متفاوت است. اما از مهمترین آنها میتوان آرسنیک، سرب،
کادمیم و جیوه را نام برد. این مواد از طریق پساب کارخانجات کاغذسازی،
پلاستیکسازی، مواد دفع آفات گیاهی و استخراج معادن وارد آبهای جاری و
محیط زیست میشوند.
از مهمترین فجایع آلودگی با جیوه به فاجعه آلودگی آب
رودخانه میناماتا در ژاپن با ترکیبات ارگانومرکوریک که به عنوان
کاتالیزور در کارخانه پلاستیکسازی استفاده میشود، میتوان اشاره کرد که
در آن مردم اطراف رودخانه به بیماری ناشناختهای دچار شدند که ناشی از وجود
جیوه فراوان در بدن آنها بود و هزاران نوزاد ناقص و مرگ شمار زیادی از
مردم، پیامد آلودگی آب با پساب این کارخانه بود.
پسابهای کشاورزی
در
این پسابها، سمهای کشاورزی مانند هیدروکربنهای هالوژندار، DDT،
آلودین، ترکیبهای فسفردار مانند پاراتیون وجود دارد. ترکیبات هالوژندار
بسیار خطرناکند و هنگامی که همراه با آب کشاورزی در لایههای زمین نفوذ
نمایند یا به بیرون از محیط کشاورزی هدایت شوند، پسابهای کشاورزی بسیار
خطرناک تولید میکنند.
پسابهای شهری
این پسابها
از مصرف خانگی آب حاصل میشوند. در این پسابها انواع موجودات ریز،
میکروبها و ویروسها و چند نوع مواد شیمیایی معین وجود دارد که بیشترین آن
آمونیاک و نیز مقداری اوره میباشد. این پسابها باید از مسیرهای سربسته
به محل تصفیه هدایت گردند. برای خنثا سازی محیط قلیایی این پسابها که برای
رشد و نمو میکروبها محیط مناسبی است، از کلر استفاده میشود.
انواع آلایندههای موجود در پسابهای شهری
آلایندههای زیستی: از دفع پسابهای بیمارستانی و مراکز بهداشتی شهری ناشی میشود.
آلایندههای
شیمیایی: آلایندههای شیمیایی پسابهای خانگی بیشتر ناشی از مصرف
شویندههاست که روز به روز مصرف آنها بیشتر میشود. این آلایندهها بهعلت
وجود عامل حلقوی در ساختمان ملکول شوینده (ABS)، غیر قابل تجزیه بیولوژیکی
در تصفیهخانهها هستند.
فرمول عمومی: LABS): linear Alkyl Benzo Sulfuric acid = RŔ/ (C6H5) SO3H)
امروزه
در کشورهای ژاپن و آمریکا، شوینده حلقوی را به خطی تبدیل نمودهاند که
قابل تجزیه بیولوژیکی در تصفیهخانههاست. ولی در بیشتر کشورها به علت
ارزان بودن (LABS) هنوز هم این ماده در شویندهها به کار میرود.
سایر آلایندهها: مواد جامد و رسوبات، مواد رادیواکتیو، مواد نفتی و آلایندههای گرمایی مانند نیروگاهها.
پسابهای غیر انسانی
باید
دانست که در طبیعت تنها انسان نیست که با تولید پساب آبها را آلوده
میکند. بلکه فعالیت جانوران نیز در این آلودهسازی نقش دارد. اگر میزان
آلودگی انسان را معادل یک BOD فرض کنیم، جانوران دیگر مانند اسب، گاو،
گوسفند، خوک و مرغ خانگی به ترتیب 11.3، 16.4، 2.5، 1.9 و 0.91 خواهند بود.
آلودگی آب در جهان
حدود 69 % آب مصرفی جهان، صرف
کشاورزی و آبیاری میشود. 23 % به مصرف صنایع میرسد و مصارف خانگی تنها
حدود 8 % را شامل میشوند. در کشورهای پیشرفته، کشاورزی و صنایع بیشترین
مصرف آب و بالاترین نقش را در آلودگی آبها دارند.
برای گرد آوری اطلاعات کیفی آب بیش از 50 پارامتر تعریف شده است که مهمترین آنها عبارتند از:
Do
(اکسیژن محلول)، BoD (اکسیژن مورد نیاز واکنشهای بیوشیمیایی)، CoD
(اکسیژن مورد نیاز واکنشهای شیمیایی)، میزان کلروفرمها و نیتراتها و
فلزهای سنگین میباشد.
درجهبندی پسابها
پسابها بر پایه مقدار BOD
درجهبندی میشوند. پسابهایی که BOD آنها به ترتیب در حدود 210، 350 و 600
میلیگرم در لیتر است، پسابهای ضعیف، متوسط و قوی هستند. برای جلوگیری از
آلودگی آبها در بیشتر نقاط جهان ، هیچ پسابی حتا پس از تصفیه در صورتی که
BOD آن بیش از 20 میلیگرم در لیتر باشد، مجاز به ورود به جریانهای سطحی و
یا زیر زمینی نیست.
تخلیه بیرویه پسابهای صنعتی در آبهای سطحی
تخلیه بیرویه و
پسابهای صنعتی (و همین طور غیر صنعتی و کشاورزی) در آبهای سطحی، موجب مرگ
و میر جانوران آبزی میگردد. جالب توجه است که تلاشی اجساد همین جانوران
خود مزید بر آلودگی هر چه بیشتر میگردد. از دیگر اثرات مهم این فاجعه
تبدیل فعالیت باکتریهای آب از حالت هوازی (Aerobic) یعنی همراه با مصرف
اکسیژن به حالت بیهوازی (Anaerobic) و بدون نیاز به اکسیژن میباشد.
فعالیت باکتریهای بیهوازی، با پیدایش بوی نامطبوع و زنندهای همراه است و
بیشتر محصولات به دست آمده از فعالیت باکتریهای بیهوازی برای زندگی
جانداران دیگر زیانآور است.
تصفیه آب و پسابها
آب و پسابها برای استفاده و
برای برگشت به محیط یا استفاده دوباره نیاز به تصفیه دارند. روشهای
گوناگونی برای تصفیه آبها و پسابها وجود دارد که بسته به مصارف آب و نوع
آلودگی از این روشها استفاده میشود. عمدهترین روشهای تصفیه آب عبارتند
از:
تصفیه مکانیکی آب
تصفیه شیمیایی آب
تصفیه آب به روش اسمز معکوس
تصفیه بیوشیمیایی آب
فیلتراسیون آب
پتانسیل اکسیداسیون
پتانسیل اکسیداسیون، یکی از معیارهای مهم برای
اندازهگیری آلودگی آبهاست. اکسیژن محلول در آب، عامل اساسی زندگی و رشد
جانوران و گیاهان است. زندگی این موجودات به حداقل اکسیژن محلول در آب
بستگی دارد. ماهی بیش از سایر جانداران و بیمهرهگان در درجه دوم و
باکتریها کمتر از تمام موجودات آبزی به اکسیژن محلول در آب نیاز دارند. در
یک آب معمولی که ماهی در آن پرورش مییابد، اکسیژن محلول نباید از 5
میلیگرم در لیتر کمتر باشد و این مقدار در آبهای سرد به 6 میلیگرم در
لیتر افزایش مییابد.
اگر مقدار اکسیژن محلول در آب از کمینه مجاز برای
زندگی جانداران آبزی کمتر باشد، آب آلوده تلقی میگردد. وجود مواد آلی در
آب، موجب مصرف و کاهش مقدار اکسیژن محلول میگردد. بیشتر ترکیبات آلی موجود
در آب دارای کربن هستند و در واکنش مهمی که در محیط آبی به کمک باکتریهای
خاصی انجام میپذیرد به ترتیب زیر است، به ازای 12 گرم کربن، 32 گرم
اکسیژن مصرف میشود. اگر فرض کنیم که مقداری روغن که حاوی 12 گرم کربن است،
در آب ریخته شود، با در نظر گرفتن حداکثر مقدار اکسیژن محلول در آب در
شرایط معمولی (میلیگرم در لیتر) این مقدار روغن، آبی در حدود 3555 لیتر را
فاقد اکسیژن و کاملا آلوده مینماید.
اکسیژن مورد نیاز جهت اکسیداسیون پساب
اکسیژن مورد نیاز جهت
اکسیداسیون پساب معیار مناسبی برای آگاهی از حدود مقدار مواد آلاینده موجود
در آن است. دو روش تعیین میزان آلودگی که بر اساس یاده شده در بالا متکی
هستند، تحت عناوین COD و BOD شناخته شدهاند.
(BOD (Biochemical Oxygen Demand:
BOD
عبارت است از میزان اکسیژن مور نیاز میکرو ارگانیسمها در اکسیداسیون
بیوشیمیایی مواد آلی موجود در آب. در حقیقت BOD تعیینکننده مقدار اکسیژن
مورد نیاز برای ثبوت بیولوژیکی مواد آلی نمونه مورد نظر خواهد بود. اگر BOD
آبی در حدود 1 میلیگرم در لیتر باشد، آب خوب و اگر به حدود 3 برسد مشکوک و
بیشتر از 5، آلوده است.
(COD (Chemical Oxygen Demand:
COD عبارت
است از میزان اکسیژن مورد نیاز برای اکسیداسیون مواد قابل اکسیداسیون موجود
در آن. مقدار COD معمولا با استفاده از یک اکسنده قوی در محیط اسیدی قابل
اندازهگیری است.
تعیین BOD با وجود ارزش فراوان، دو ضعف اساسی دارد؛
یک: طولانی بودن مدت آزمایش و دو: امکان مسموم شدن میکرو ارگانیسمها در
تماس با مواد آلوده در این مدت طولانی. از این رو، COD ارزش فراوانی دارد.
17 الف) خاک دياتومه (Diatomaceous earth) از بقاياي
فسيل جلبکهاي تک سلولي به نام دياتوم بوجود آمده است. خاکهاي دياتومه با
توجه به مواد سازنده به رنگهاي گوناگون از سفيد تا خاکستري يا زرد و قرمز
ديده ميشوند و در اشکال متفاوت گرد، پهن و مسطح وجود دارند. فرم پهن
خاکهاي دياتومه سطح فعال بيشتري دارد.
خاکهاي دياتومه از دياتومهايي
با منابع متفاوت به وجود آمدهاند. مقدار کريستال سيليکاي موجود در خاک
دياتومه نقش بسزایی در قدرت حشرهکشي آنها ايفا ميکند. به طور کلي
خاکهاي دياتومهاي که از دياتومهاي آبهاي درياها پدید آمدهاند 2 تا 7
درصد کريستال سيليکا دارند و خاکهاي دياتومهاي که از دياتومهاي آبهاي
شيرين (برکه، درياچه، مرداب) ايجاد شدهاند محتوي کمتر از 1 درصد کريستال
سيليکا ميباشند.
افزون بر اين، اندازه ذرات خاکهاي دياتومه نيز در
توانايي حشرهکشي آنها مهم است. ميانگين اندازه ذرات تشکيلدهنده خاکهاي
دياتومه در صورتي که برابر و کوچکتر از 15 ميکرومتر باشد، مناسب است.
همچنین عملکرد خاک دياتومه به مقدار اکسيد سيليسيم (2SiO) موجود در آن نیز
بستگی دارد.
طرز کار خاک دياتومه
ذرات خاک دياتومه حاوي حفرههای
ريزي هستند که توانايي جذب ملکولهاي موم اپيکوتيکول حشره را دارند. لذا
هنگام تماس با کوتيکول حشره، لايه مومي کوتيکول را جذب و به مقدار کمي بر
روي سطح کوتيکول خراش ايجاد میکند که سبب از دست رفتن آب بدن و مرگ حشره
ميشود.
نحوه کاربرد خاک دياتومه
خاکهاي دياتومه به دو صورت به کار میروند:
1- تيمار کردن انبار با خاک دياتومه پیش از ذخيرهسازي مواد غذايي
خاکهاي
دياتومه به صورت گرد و يا اسپري وتابل جهت تيمار انبارهاي خالي و وسايل
نقليهاي که براي جابهجایی مواد غذايي به انبارها استفاده میشوند، پس از
انجام اقدامات بهداشتي براي جلوگيري از ورود آفات به انبارها و ايجاد
آلودگيهاي ثانويه به کار گرفته ميشوند.
روش گردپاشي متداولتر است و
در مقایسه با روش اسپري آفات انباري را بهتر کنترل میکند. به همين دليل در
حالت اسپريپاشي براي بالا بردن عملکرد خاک دياتومه مقدار بيشتري از آن به
کار گرفته ميشود به طوري که در مورد فرمولاسيون Dryacide® خاک دياتومه
فرم گرد در حالت استاندارد به مقدار 2 گرم بر متر مربع استفاده میشود و
فرم وتابل آن به مقدار 6 گرم بر متر مربع کاربرد دارد.
2- تيمار مواد غذايي با خاک دياتومه قبل و در زمان ذخيرهسازي آن:
2-1 تيمار کل ماده غذايي با خاک دياتومه
اگر مقدار ماده غذايي انبارشده کم باشد از ابزار دستي براي مخلوط کردن خاک دياتومه با کل توده استفاده ميشود.
در
صورتي که مقدار ماده غذايي انبارشده زياد باشد چون مقدار خاک دياتومه
مصرفی در مخلوط با کل توده زياد خواهد بود لذا خاک دياتومه به دو روش به
کار میرود:
2-2 تيمار سطح رويي ماده غذايي با خاک دياتومه
خاک دياتومه فقط بر روي سطح ماده غذايي به مقدار 100 گرم در متر مربع استفاده ميشود.
2-3 تيمار عمق بالايي ماده غذايي با خاک دياتومه
مزاياي خاک دياتومه
خاکهاي دياتومه مزاياي زيادي دارند که عبارتند از:
1- کاربرد خاکهاي دياتومه آسان است.
2- خاکهاي دياتومه روي طيف گستردهای از آفات انباري اثر میگذارند.
3-
عمر انبارداري خاکهاي دياتومه نامحدود است و تا هنگامیکه سطح دانه و
انبار خشک باقي بماند از مواد غذايي انبارشده از هجوم آفات نگهداری
میکنند.
4- خاکهاي دياتومه پايدارند و بر خلاف ارگانوفسفاتها، در اثر
گرما تجزيه نمیشوند. بنابراين بقاياي شيميايي سمي روي مواد غذايي بر جا
نميگذارند و با مواد موجود در محيط زيست واکنش نشان نميدهند.
5-
گزارشهایی درباره مقاومت آفات انباري به برخي نگهدارندههاي غلات همچون
پيرتروئيدها، ارگانوفسفاتها، کارباماتها، هيدروکربنهاي کلره و برخي
سموم تدخيني وجود دارد. در صورتي که هيچ گونه مقاومتي از گونههاي انباري
به خاک دياتومه تا به حال گزارش نشده است.
6- خاکهاي دياتومه بيبو هستند.
7- خاکهاي دياتومه سميت کم روي پستانداران دارند و براي حشرههای مفيد و غير هدف کم خطر هستند.
8-
خاکهاي دياتومه هيچ گونه تاثير نامطلوبي بر قدرت جوانهزني، کيفيت، مزه،
ارزش نانوايي، خاصيت آرد و ویژگیهای دیگر دانه ندارند و استفاده از آنها
براي نگهداری غلات، بقولات و دانههاي روغني ثبت گرديده است.
9- خاکهاي دياتومه توسط سازمان محيط زيست ايالت متحده امريکا بعنوان يک ماده امن معرفي شدهاند.
10-
خاکهاي دياتومه حاوي سيليکاي بيشکل ميباشند که با توجه به گزارش آژانس
بين المللي سرطان، سيليکاي بيشکل متعلق به نسل سوم آفتکشهاست و شواهد و
مدارک کافي براي سرطانزايي آن وجود ندارد.
11- خاکهاي دياتومه دوره کارنس ندارند و بلافاصله پس از کاربرد، دانه قابل مصرف ميباشد.
12- خاکهاي دياتومه در آمريکا و کانادا به عنوان افزودني غذا ثبت گرديدهاند.
13- استفاده از خاکهاي دياتومه در مقايسه با روشهاي فعلي کنترل آفات انباري اقتصاديتر است











 و نظایر آنها در ساختن وسایل نوری بکار میروند.
و نظایر آنها در ساختن وسایل نوری بکار میروند.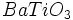 در صنعت الکترونیک کاربرد دارند.
در صنعت الکترونیک کاربرد دارند.
 نگاه کلی
نگاه کلی 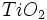 مصرفی در رنگسازی از نوع روتایل است. آناتاز را با حرارت دادن در 700-950 درجه سانتیگراد میتوان به روتایل تبدیل کرد.
مصرفی در رنگسازی از نوع روتایل است. آناتاز را با حرارت دادن در 700-950 درجه سانتیگراد میتوان به روتایل تبدیل کرد. 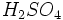 ،
، 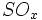 و بخار آب تولید میشود که وقتی وارد جو شوند، موجب آلودگی هوا خواهند شد.
بنابراین استفاده از تصفیه کننده در کارخانهها ضروری است. از ضایعات دیگر
این روش باز ، تولید اسید سولفوریک مصرف شده بدون برگشت آن به چرخه تولید
میباشد.
و بخار آب تولید میشود که وقتی وارد جو شوند، موجب آلودگی هوا خواهند شد.
بنابراین استفاده از تصفیه کننده در کارخانهها ضروری است. از ضایعات دیگر
این روش باز ، تولید اسید سولفوریک مصرف شده بدون برگشت آن به چرخه تولید
میباشد. 
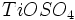
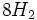
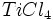 آن را تقطیر کرده و تتراکلرید تیتانیوم خالص را با اکسیژن هوا در شعلهای
با دمای 1500 درجه سانتیگراد اکسید میکنند (واکنش سوختن). دراین فرایند
دانههای بسیار ریز دیاکسید تیتانیوم و گاز کلر ایجاد میشود. کلر تولید
شده دوباره وارد چرخه تولید میشود.
آن را تقطیر کرده و تتراکلرید تیتانیوم خالص را با اکسیژن هوا در شعلهای
با دمای 1500 درجه سانتیگراد اکسید میکنند (واکنش سوختن). دراین فرایند
دانههای بسیار ریز دیاکسید تیتانیوم و گاز کلر ایجاد میشود. کلر تولید
شده دوباره وارد چرخه تولید میشود.
 از سینتیک درجه اول پیروی میکند.
از سینتیک درجه اول پیروی میکند. 



 :مولکول پر انرژی
:مولکول پر انرژی
 است.
است. 



